一次统计力学之旅
“当我们凝视一杯静止的水时,我们看到的是宏观世界的‘宁静’与‘确定’。然而,在微观层面,一场涉及
在物理学的众多分支中,统计力学拥有独特的逻辑美感。它既不需要经典力学那样复杂的受力分析,也不需要量子场论中繁琐的相互作用项。它仅仅需要一个极度简单的公理——‘统计力学的基本假设’。只要你承认,在一个孤立系统中,每一个可能的微观态出现的概率都是相等的,那么热力学宇宙的其余部分——从温度的定义到玻尔兹曼分布,从化学势的推导到玻色-爱因斯坦凝聚——都可以像推翻多米诺骨牌一样自然地推导出来。
这是一个关于‘多即不同’(More is Different)的故事。本文旨在剥离具体的复杂模型,还原热物理学的原始骨架。我们将从‘多重度函数’(Multiplicity Function)出发,以‘熵’为指引,重新追溯从微观计数到宏观预测这一奇妙旅程。”
*注:本文假设读者具备量子力学的基本知识和概念,因为统计力学在本质上是量子化的。实际上,我们是在计算海量量子所产生的统计效应。
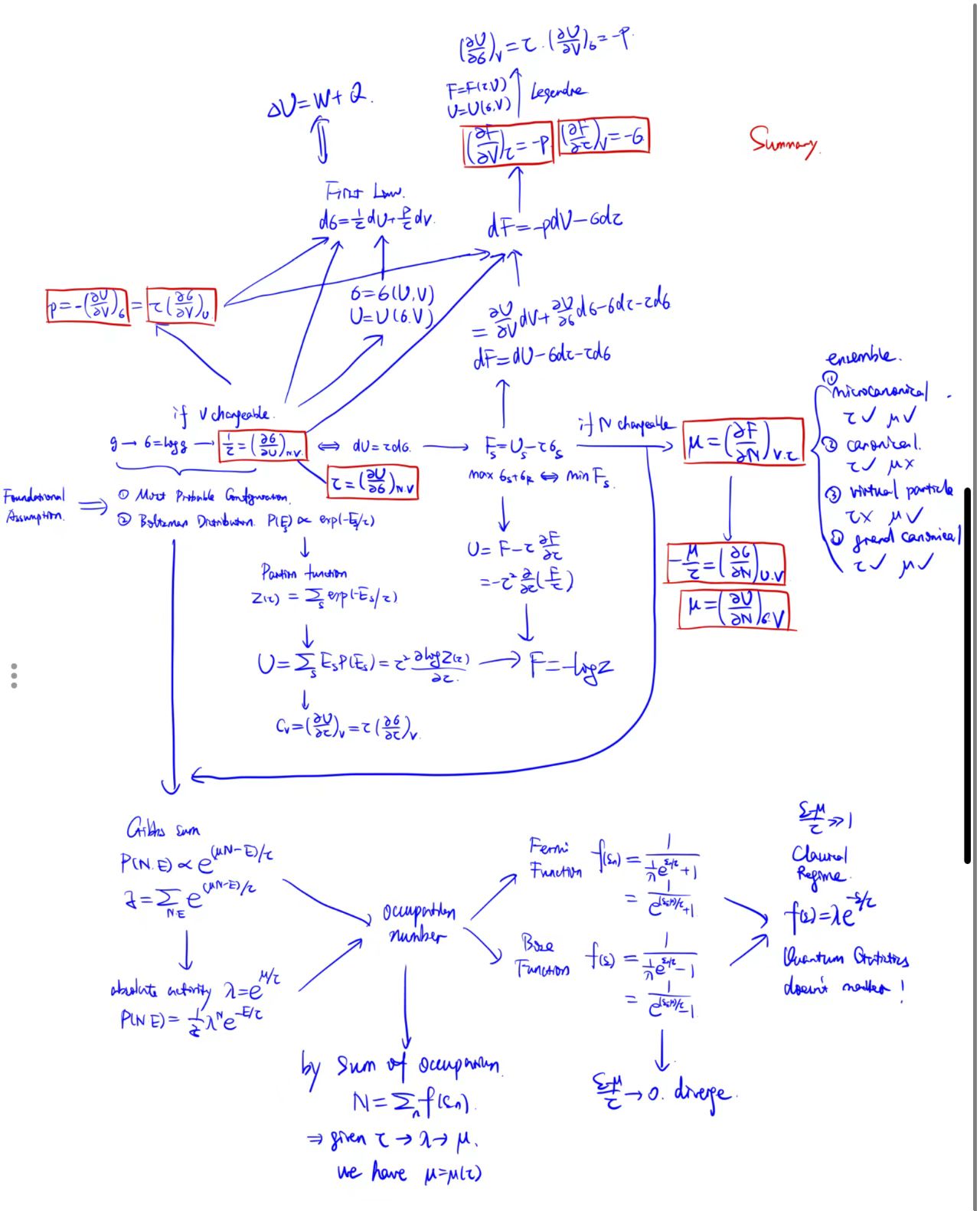
第一章:计数的艺术 —— 从多重度到热平衡
我们的旅程始于一个简单到近乎离谱的问题:在给定的宏观条件下,一个系统究竟有多少种可能的微观“生存方式”?
物理学家为这种“方式”的数量赋予了一个名字:多重度(Multiplicity),通常用符号
1. 基本假设:自然是公平的
想象一个孤立的箱子,里面装有
统计力学建立在唯一一个基础公理之上——基本假设:
对于一个孤立系统,所有满足能量守恒且可达到的量子态,出现的概率都是相等的。
这意味着大自然不偏不倚。只要能量条件允许,系统处于状态 A 的机会与处于状态 B 的机会完全相同。
2. 为什么要定义熵?(
如果多重度
这并非为了故弄玄虚,而是出于两个极其务实的原因:
- 数值过于庞大:对于宏观物体,
是一个天文数字。即使是一小瓶气体, 的数量级也可能达到 。处理这样的数字不仅麻烦,而且在数学上不直观。 - 我们需要“可加性”(Additivity):想象你有两杯水,系统 A 和系统 B。
- 如果你将它们视为一个整体,总状态数是各自状态数的乘积:
(组合原理)。 - 然而在宏观物理中,我们习惯于“加法”。质量是相加的,体积是相加的,能量也是相加的。我们希望这个描述“无序程度”的量同样满足相加关系。
- 如果你将它们视为一个整体,总状态数是各自状态数的乘积:
什么数学工具能将乘法转变为加法,同时将巨大的指数驯服为易于处理的数字?答案是对数。
因此,玻尔兹曼(和普朗克)给出了物理学中最深刻的定义之一——基本熵(Fundamental Entropy):
熵,在本质上,就是微观态数量的对数。它不是某种神秘的破坏力;它仅仅是我们对系统“可能性”的一种度量。
3. 为什么热平衡意味着熵最大化?
现在,让我们见证奇迹时刻。
假设我们将两个独立的系统 A 和 B 放在一起,并允许它们进行热接触(Thermal Contact)。这意味着它们可以交换能量,但总能量
系统会如何演化?
根据基本假设,系统会进行“随机游走”,尝试各种能量分布。然而,有一种分布的概率将压倒性地统治其他所有分布——那就是让总微观态数量
从数学上讲,最大化
仅利用统计力学的单一基本假设,整个系统的多重度为
现在,如果我们考虑到只有_概率最大的配置_对
结论: 系统向热平衡演化,是因为平衡态拥有最多的微观态数量。熵增,从根本上说,是系统向着“更多可能性”的方向演化。
4. 温度的诞生:为什么将其定义为导数?
当两个系统达到热平衡(熵最大化)时,会发生什么?根据微积分,当一个函数达到极值时,其导数为零。
我们对能量分布求总熵的导数:
由于能量守恒(
将其代回,我们得到至关重要的平衡条件:
停下来思考一下:
当两个物体达到热平衡时,什么物理量是相等的?直觉告诉我们是温度。
这意味着数学量
让我们看看这个量的物理含义:它是“熵随能量的变化率”。
- 当你给一个冷物体一点能量时,它的无序度(状态数)会剧烈增加。冷物体对能量非常“饥渴”(
很大)。 - 当你给一个热物体一点能量时,其无序度的增加微乎其微。热物体对能量表现得“无所谓”(
很小)。
既然较大的
因此,为了符合人类的认知习惯,我们将基本温度 (
这就是统计力学中温度的严谨定义:温度衡量的是系统为了增加熵而愿意“支付”能量的意愿。
- 低迷温度意味着极小的能量投入就能换取巨大的熵增(高性价比)。
- 高温则意味着即使投入大量能量,熵的增加也微乎其微。
如果仔细观察,你会发现温度的定义与半衰期具有相似的形式;正如半衰期与时间具有相同的量纲,温度(在自然单位制下)与能量具有相同的量纲。
第二章:压强的诞生
1. 为什么熵是
首先,我们必须回答一个元问题:为什么我们总是将熵写成
(能量): 决定了你可以分配给粒子运动的“预算”。 (体积): 决定了粒子可以占据的“空间”(在量子力学中,体积决定了驻波的波长,即能级结构)。 (粒子数): 决定了有多少个“演员”参与这场混沌的演出。
由于
2. 压强:对空间扩张的渴望
想象一下,将我们的刚性容器换成一个装有活塞的圆柱体。现在,体积
当体积改变时,量子力学告诉我们能级实际上会发生位移:
- 考虑到统计力学,我们计算统计平均值:
。由于 ,我们得到 。 - 从另一个角度来看,能量的变化是压强所做的功:
。 - 因此,我们得到
。负号的存在是因为压强做正功会导致体积减小。
还有另一种非平凡的方法来描述压强:
本质上,压强代表了“通过扩张体积来增加熵的欲望”的强度。毕竟,当体积稍稍增加(
第三章:视角的转变 —— 为什么要引入自由能?
我们已经拥有了熵函数
当我们从“孤立系统”(固定
1. 亥姆霍兹自由能(Helmholtz Free Energy)
假设两个系统处于热接触状态。一个是巨大的热库(Heat Reservoir),另一个是我们关注的系统(固定体积
- 由于平衡时温度相等,
,故 ,导致 。这就是为什么我们这样定义 ——为了寻找一个极值。回想一下,对于系统和热库而言,平衡条件是使 最大化。我们实际上并不关心热库,而最小化系统的自由能 为我们提供了一种忽略热库、同时仍能确定平衡状态的方法。让我们证明它是最小值。 - 总熵为
。由于热库巨大,我们进行泰勒展开: 。显然,最大化熵等同于最小化自由能。注意,熵属于“系统+热库”,但自由能仅属于系统。 。这是一个优美的结果。有了自由能,我们可以撇开热库。热库仅贡献了一个 ,这在平衡时是一个固定的常数。
2. 化学势:粒子流动的驱动力
现在我们释放最后一个变量:粒子数
- 关键在于,
。 - 回想自由能
必须最小化( ),我们有 ,这意味着 。
我们引入弱耦合假设(Weak Link Assumption):假设管道足够细,使得两个系统在统计上是独立的(因此
- 因此,
。这就是平衡条件。 - 由此,我们定义化学势:
。
你可能会问,既然定义似乎需要两个系统,那么单个系统是否需要化学势?事实上,我们可以类比温度:
- 一个孤立的封闭系统既不需要
也不需要 。这就是微正则系综(microcanonical ensemble)。 - 如果该系统接触热库,我们需要
但不需要 来描述它。这就是正则系综(canonical ensemble)(传统热物理中最常见的)。 - 如果该系统接触粒子库,我们不需要
但需要 。虽然这类系统确实存在(粒子是“虚拟”的,不携带能量,比如信息),但在标准物质物理中很少见。 - 如果系统同时接触热库和粒子库,我们需要
和 。这就是巨正则系综(grand canonical ensemble)。
此前,压强的定义是从能量
第四章:热力学恒等式 —— 同一真理的不同面孔
我们已经定义了熵、温度、压强和化学势。现在,我们进入这座大厦的内部,探索这些物理量之间错综复杂而又对称的关系。通过微分的艺术,我们将揭示热力学第一定律的本质,并展示如何通过数学变换在不同的“能量景观”中穿梭。你会发现,热物理学不像经典力学那样只有单一的核心定律(
1. 书写第一定律的三种方式
让我们玩一场微分游戏,看看从不同的函数出发会得到什么结果。
视角 1:熵
如果我们把熵视为内能和体积的函数,其全微分为:
回想我们的定义:
等式两边同乘
或者写成熟悉的格式:
视角 2:内能
如果我们反转视角,将内能视为熵和体积的函数:
这仍然是第一定律,但观察点发生了偏移:温度是内能对熵的斜率,而压强是内能对体积的斜率。
视角 3:自由能
这是最精妙的一步。回想
代入
项
这意味着如果我们把
2. 核心真理:
面对这么多公式,你可能会问:热物理学的核心是什么?是否存在一个像
- 能量交换:
- 体积交换(通过可移动隔板):
- 粒子交换(通过多孔隔板):
系统何时达到平衡?当总熵达到最大值时,即
展开微分项:
利用守恒关系
由于
- 能量平衡:
(温度相等) - 体积平衡:
- 粒子平衡:
关键洞察: 严格来说,平衡的条件是
和 的相等。只是因为我们通常同时也交换能量(使得 相等),才得到了熟悉的 和 。所有的热力学量本质上都源于极值条件 。
3. 共轭变量 —— 舞伴
如果我们回顾内能
这揭示了物理量总是成对出现的,每一对都包含一个广延量和一个强度量,被称为共轭变量(Conjugate Variables):
| 广延变量 (Extensive) | 强度变量 / 广义力 (Intensive) | 物理意义 |
|---|---|---|
| 熵 |
温度 |
|
| 体积 |
压强 |
|
| 粒子数 |
化学势 |
这为我们通过经典力学(力平衡)理解热物理提供了一个新视角:热平衡本质上是广义力的静态平衡。
4. 勒让德变换 —— 变换主语
最后,我们从数学上解释为什么
(注意:这里的
由于
这就是对偶性(Duality)的魔力:它将自变量从
(新得到的) (保持不变) (保持不变)
我们现在已经导出了所有的热力学关系,并理解了为什么自由能是一个量身定制的势函数,以适应那个“温度比熵更容易控制”的现实世界。
第五章:热物理学的罗塞塔石碑
经过前四章的探讨,我们分别从三个视角审视了系统:微观计数(熵)、能量守恒(内能)以及实用主义(自由能)。这就像“盲人摸象”——不同的部位,不同的描述。如果我们将这三个势函数
| 物理量 | 熵表示 σ(U,V,N) | 内能表示 U(σ,V,N) | 自由能表示 F(τ,V,N) |
|---|---|---|---|
| 温度 |
|||
| 压强 |
|||
| 化学势 |
我们必须从这张表中解读出三层信息。
1. 对角线上的“定义”
虽然每一个等式在数学上都是成立的,但物理学家通常习惯利用从左上角到右下角的对角线来确立定义:
- 第一行第一列:
。这是温度的统计力学定义。 - 第二行第二列:
。这是压强的力学定义(广义力)。 - 第三行第三列:
。这是化学势的实际定义(在恒温 下增加一个粒子引起的自由能变化)。
2. “唯一的真理”与冗余
你需要背诵所有这 9 个公式吗?不。后两列在技术上是“冗余”的。所有的物理学内容都包含在第一列(熵)之中。
- 一旦你拥有了
,你就拥有了整个宇宙。 - 第二列(
)仅仅是它的反函数。 - 第三列(
)仅仅是它的勒让德变换。
物理学家保留它们并非为了提供新信息,而是为了坐标变换的便利性(在现实中,保持
3. 数学桥梁
如何从第一列推导出第二列?这纯粹是微积分的功劳。
**桥梁 1:倒数关系(Reciprocal Relation)**对比第一行:
**桥梁 2:循环关系(Cyclic Relation)**对比第三行:
令
代入第二列的定义(分子为
第六章:大逆转 —— 从配分函数到吉布斯求和
在前几章中,我们通过微观计数 (
- 概念逻辑:
。 - 计算逻辑:
通常极难计算(想象一下计算 个粒子的排列组合)。
因此,物理学家发明了一条“反向通道”:编写能量模型,计算配分函数 (
1. 玻尔兹曼分布
考虑系统
利用
信息熵视角:
如果我们在仅已知平均能量的情况下,寻求最“无偏”的概率分布(即最大化香农熵 ),利用拉格朗日乘数法同样可以导出 。玻尔兹曼分布是自然界最“自然”、最无偏的选择。
2. 配分函数:统计力学的“圣杯”
为了归一化
因此
计算逻辑的“大回旋”:
- 列出微观模型(能级
)。 - 求和计算
(通常通过几何级数或高斯积分)。 - 求出自由能
( )。 - 推导一切(通过对
求导得到 )。
3. 吉布斯求和:当粒子流动时
如果系统也交换粒子(巨正则系综),热库的熵
这导出了吉布斯分布:
归一化常数即为巨配分函数,也称吉布斯求和 (
定义绝对活性
一个悖论? 在玻尔兹曼分布中,
第七章:量子统计 —— 当粒子失去姓名
最后,我们来处理那个绕不开的问题——量子力学。此前,我们将粒子视为可以区分的“小球”。现在,我们必须面对**全同性(不可区分性)**的现实。
1. 它是谁?不,它是什么?
在量子世界中,同类粒子在根本上是不可区分的。交换两个粒子,其概率密度
- 玻色子 (+1): 具有社交倾向,喜欢聚在一起(如光子、氦-4)。
- 费米子 (-1): 具有反社交倾向,遵循泡利不相容原理,绝不占据同一状态(如电子、质子)。
**计数的改变:**将 2 个粒子放入 4 个能级中:
- 经典情况:
种方式。 - 玻色子: 10 种方式(在一起的概率增强)。
- 费米子: 6 种方式(在一起的概率为零)。由于多重度
改变了,熵 和宏观性质也随之改变。
2. 从粒子视角到轨道视角
与其询问“粒子 A 在哪里?”,不如询问“能量为
3. 费米-狄拉克分布与玻色-爱因斯坦分布
**费米子:**占据数
平均占据数:
分母中的
**玻色子:**占据数
平均占据数:
如果
4. 经典极限:殊途同归
为什么我们日常感觉不到这种差异?因为我们生活在经典区间:高温或低密度(即
这正是玻尔兹曼分布!然而,当我们冷却到量子浓度 (
结语:从无知中涌现的秩序
我们的旅程在此告一段落。让我们回顾一下建立起来的体系:
- 我们从承认“无知”出发:即等概率原理。
- 我们通过计数和熵量化了“可能性”。
- 通过最大化熵,我们发现温度、压强和化学势这些宏观岛屿从混沌的微观海洋中涌现。
- 我们利用自由能指引航向,并将配分函数作为罗盘。
- 最后,注入量子特性,该框架预言了极端条件下的物质状态。
值得注意的是,我们几乎没有提到具体的物质。我们没有计算铜的比热或氧分子的转动。这就是统计力学的魅力:它是一套普适的语法,而不是一个特定的故事。
它描述的是“多”的逻辑,而非“一”的身份。无论是气体分子、腔内的光子,还是恒星内部的核物质,只要你输入哈密顿量,宏观性质就会自动涌现。
什么是热物理学?
它是关于“多”的科学。它讲述了当无数微小的个体聚集时,一种全新的、确定性的宏观秩序如何通过统计法则产生——这种秩序是个体本身所不具备的。
这或许是物理学中最深刻的诗意:上帝不需要掷骰子,混沌本身就是秩序的源泉。